Natrium reagiert heftig mit Wasser
Metallisches Natrium reagiert - laut Angaben - heftig mit Wasser. Wir machen den Test und überprüfen was dran ist. Ca. 100 g Natrium werden dabei in Wasser zur Explosion gebracht.Natrium unter Parafinöl um vor Luft und Feuchtigkeit zu schützen (Bild: Wikipedia / Superplus)
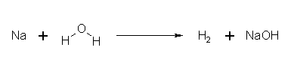
Die folgende Reaktionsgleichung zeigt, wie Natrium mit Wasser unter Bildung von gasförmigem Wasserstoff und Natriumhydroxid reagiert:
Reaktionsgleichung: Natrium + Wasser bilder Natriumhydroxid
Hier sehen wir auch alles, was es zur Erklärung bedarf: Es bildet sich bei der Reaktion das stark ätzende Natriumhydroxid, welches in Wasser gelöst die bekannte Natronlauge ergibt. Genau diese entsteht bei Berührung auf der Haut durch die Reaktion mit feinen Schweißtröpfchen.
Warum aber explodiert das Alkalimetall wenn es in Kontakt mit größeren Mengen an Wasser kommt?
Nehmen wir an, wir werfen ein 100 g Stück Natrium in ein Schwimmbecken (ohne Schwimmer natürlich!): Bei der o. gezeigten Reaktion wird sehr, sehr viel Reaktionswärme frei, d.h. das Metall und das umgebende Wasser erhitzen sich rasch. Natrium schmilzt bereits bei 98 °C. Die Temperatur wird schnell erreicht. Als Schmelze (Pfütze) hat Natrium auf dem Wasser eine größere Kontaktfläche und kann jetzt noch besser reagieren. Gleichzeitig wird Wasser verdampft, was ebenso schneller reagiert, als das flüssige Wasser - es wird rapide heißer.
Ab hier können mehrere Reaktionen gleichzeitig ablaufen: Natrium kann unter Anwesenheit von Wasser explosive Peroxide bilden oder es wird so heiß, dass die Zündtemperatur von Wasserstoff bzw. korrekter gesagt Knallgas (Wasserstoff + Sauerstoff) erreicht wird. Das Metall beginnt zu brennen! Ein Metallbrant ist i.d.R. mehrere tausend Grad heiß und kann nur durch Sand gelöscht werden - Ein Feuerlöscher versorgt die Flamme lediglich mit brennbarer Nahrung und der Flammenherd wird noch heftiger: Wer versucht, einen Metallbrand mittels CO2-Löscher zu tilgen, der erlebt eine Stichflamme!
Weiter in der Erklärung: Bei 883 °C verdampft Natrium. Als Dampf bietet die Substanz die größte Reaktionsoberfläche und reagiert deswegen um ein vielfaches schneller, denn als Feststoff. Das dampfförmige Natrium reagiert mit dem ebenso dampfförmigen Wasser schlagartig in einer heftigen Knallgasexplosion. Das folgende Video zeigt den Verlauf dieser Reaktion:
Das nächste Video zeigt eine etwas größere Menge an Natrium (ca. 100 g), die ohne vorheriges Zünden schlagartig abreagiert...
Es muss wohl nicht erwähnt werden, dass man sich mit der Materie gut auskennen sollte, bevor man auf den Gedanken kommt Derartiges selbst auszuprobieren. Also liebe Kinder (und erwachsene Kinder): Lasst die Finger davon!
Bildquelle:
johannes flörsch
(So findest du die Sternschnuppen der Perseiden)
Karin Scherbart
(Wie macht man einen Regenbogen selbst?)