Wie funktioniert eigentlich Seife?
Das Wirkprinzip von Seife ganz einfach und detailliert erklärt.Polare und unpolare Moleküle
Polare Moleküle sind sozusagen winzige Magnete. Es spielt keine Rolle, wie die Form und Farbe dieser Magnete ist: sie ziehen sich gegenseitig an und bilden eine einheitliche Materie. Unpolare Moleküle kann man sich als nicht-magnetische Plastikteile vorstellen.  Das Plastik wird von Magneten nicht angezogen und mischt sich daher auch nicht mit der Magnetenmenge, wenn man versucht beide Komponenten zu vereinigen.
Das Plastik wird von Magneten nicht angezogen und mischt sich daher auch nicht mit der Magnetenmenge, wenn man versucht beide Komponenten zu vereinigen.
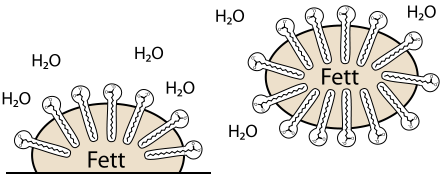
Seifenmoleküle, auch Tenside genannt, vereinen beide Eigenschaften: Ein kleiner magnetischer Teil ist an einen nicht-magnetischen Plastikrest gebunden. Der Vergleich hinkt aus chemischer Sicht ein wenig, aber das Prinzip ist beinahe übertragbar. Man muss sich jetzt nur noch vorstellen, dass sich die Plastikteile auf molekularer Ebene gegenseitig ebenso anziehen wie die Magneten. Die Seifenmoleküle binden also auf der einen Seite an die polaren Wassermoleküle (Magnetischer Teil) und auf der anderen Seite an Fett- und Ölpartikel (Plastikteil) und ermöglichen damit die Mischung von den ursprünglich unmischbaren Substanzen. Im folgenden Bild wird dies gezeigt. H2O ist das Wasser, die Stäbchen sind die Tensidmoleküle, wobei die runden Köpfe die polaren "Magnete" der Seifenmoleküle darstellen.
Seifenmoleküle: Tenside haben einen wasserlöslichen und einen fettlöslichem Teil und binden damit polare und unpolare Stoffe
Für die, die lieber lesen
Bildquelle:
johannes flörsch
(So findest du die Sternschnuppen der Perseiden)
Karin Scherbart
(Wie macht man einen Regenbogen selbst?)